Яблоки являются самым привычным, доступным и востребованным фруктом в средней полосе России. Это объясняется как их полезными свойствами, так и возможностью длительного хранения в свежем, консервированном или переработанном виде. Яблоки представлены на потребительском рынке г. Самара несколькими сортами, конкурентоспособность которых определяется их пищевой ценностью и отсутствие вредных веществ.
Пищевая ценность яблок связана с содержанием в них белков, жиров, углеводов, витаминов и минералов. Основным полезным веществом в составе яблок является железо, содержание которого одно из самых больших по сравнению с другими овощами и фруктами (около 2,2 мг на 100 г яблока).
Вредные вещества поступают в плоды яблок из окружающей среды (почва, вода, воздух). В составе плодов содержится 84-90% воды, вернее яблочного сока, содержащего до 95% воды, которая способна растворять эти вещества.
Содержание железа, а также отсутствие вредного содержания нитратов являются основными критериями определяющими конкурентоспособность различных сортов яблок, как товара массового потребления. Контроль этих веществ в различных сортах яблок, представленных на потребительском рынке г. Самары, являлся целью настоящей работы.
Анализ проводили в водных вытяжках яблок по методикам, разработанным на кафедре АиФХ ФГБОУ ВПО «СамГТУ».
Анализ содержания железа
Анализ содержания железа основан на фотометрическом определении содержания железа в растворе путем сравнения его светопоглощения (оптической плотности) со светопоглощением стандартного раствора с известным содержанием железа. Для обеспечения необходимой величины светопоглощения растворы, содержащие железо, окрашивают в красно-оранжевый цвет с помощью реакции комплексообразования ионов железа (III) с тиоцианат-ионами CNS-.
Приборы и реактивы
- Фотоколориметр КФК-2 или другой марки;
- Колба мерная на 100 мл -1 шт;
- Цилиндр мерный на 20 мл — 1 шт;
- Пипетка градуированная на 1-5 мл;
- Капельная пипетка — 1 шт;
- Химический стакан на 300 мл -1шт;
- Кислота азотная концентрированная;
- Раствор смеси KCNS (10%) и H2SO4 (1М);
- Стандартный раствор железа (III) c T(Fe) = 0,0005 г/cм3.
Ход анализа
1. Приготовление водной вытяжки яблока. Яблоко примерно 5 г натирают на терке в ванночку. Взвешивают. Массу яблока переносят в стакан на 300 см3. Ванночку опять взвешивают. По разности определяют массу тертого яблока, взятой для анализа.
В стакан с массой яблока добавляют 30 см3 дистиллированной воды и 0,5 г NH4Cl, кипятят 3 мин. Немного охладив, центрифугируют в течение 5 мин. Сливают раствор в мерную колбу на 100 см3, осадок при этом остается в пробирке, к нему приливают 10 см дистиллированной воды с добавлением 0,5 г NH4Cl. Центрифугируют в течение 5 мин. Раствор опять сливают в мерную колбу. Операцию промывки осадка повторяют еще раз.
В мерную колбу, где находится раствор и промывные воды, добавляют 1 см3 HNО3, 10 см3 смеси KCNS + H2SО4, доводят водой до метки, перемешивают и фотоколориметрируют по аналогии со стандартным раствором.
Приготовление стандартного раствора железа.
В мерную колбу вместимостью 100 см3 наливают из бюретки 10 мл исходного стандартного раствора Fe (III) c T(Fe) = 0,5 мг/cм3. Полученный раствор доводят до метки водой, добавляют 1 см3 HNО3 и 10 см3 смеси KCNS + H2SО4, доводят до метки водой, раствор тщательно перемешивают. Титр стандартного раствора равен 0,05 мг/см3.
Фотометрический анализ по методу сравнения.
Полученные исследуемый и стандартный растворы фотометрировали с использованием сине-зеленого светофильтра (λ = 490 нм), кюветы на 5 мм. Регистрируют величину оптической плотности Ах и Аст.
Полученную оптическую плотность Ах используют для расчета концентрации (мкг/кг) железа по формуле:
где Vст — объем стандартного раствора, взятого для приготовления раствора сравнения, mnav — масса навески яблока.
Фотометрическими измерениями было получено:
- для стандартного Аст = 0,305;
- для испытуемых водных вытяжек представлены в табл. 1.
№ | Сорт яблок | Масса навески, г | Светопоглощение Ах | Содержание железа, мг/кг |
1 | «Молдавия» | 5,390 | 0,112 | 17,03±0,13 |
2 | «Грени» | 4,597 | 0,099 | 17,65±0,16 |
3 | «Жигулевка» | 4,607 | 0,080 | 14,23±0,63 |
4 | «Александровка» | 4,251 | 0,097 | 18,70±0,17 |
5 | «Дочь папировки» | 4,843 | 0,098 | 16,59±0,15 |
6 | «Спартак» | 4,690 | 0,107 | 18,70±0,15 |
7 | «Гольден» | 4,715 | 0,140 | 24,34±0,76 |
8 | «Айдаред» | 4,569 | 0,137 | 24,57±0,32 |
9 | «Куйбышевское» | 4,892 | 0,085 | 15,11±0,56 |
10 | «Мантуан» | 4,956 | 0,119 | 21,16±0,18 |
Анализ содержания нитрат-иона
Анализ содержания нитрат-иона основан на ионометрическом измерении потенциала электрода, зависящего от содержания нитрат-иона. Ионометрическое определение концентрации NO3¯-ионов в сельхозпродуктах проводят в их соке или водной вытяжке, используя NO3¯-селективный электрод. Содержание нитрат-ионов находят по градуировочному графику E = f(pNО3), построенному с помощью серии стандартных растворов. Молярную концентрацию NO3¯ в испытуемом растворе (соке) находят, используя найденную для него по градуировочному графику величину pNО3, по формуле:
, моль/л.
Затем рассчитывают титр испытуемого раствора:
, г/л.
После этого рассчитывают содержание NO3¯-иона в мг на 1 кг сельхоз-продукта и сравнивают полученное значение концентрации с предельно допустимым (ПДК), руководствуясь справочными данными. Для яблок оно составляет 60 мг на 1 кг яблок.
Приборы и реактивы
- Универсальный иономер ЭВ-74;
- Стандартный 0,1М раствор KNO3;
- Пипетка аналитическая на 10 мл;
- Колбы мерные на 100 мл, 5 шт;
- Стакан химический на 50 мл, 5 шт;
- Тёрка;
- Весы технохимические;
- Центрифуга.
Ход анализа
Приготовление стандартной серии растворов KNO3
Для построения градуировочного графика готовят последовательным разбавлением исходного 10-1 М раствора KNO3 серию стандартных растворов KNO3 с концентрациями 10-2; 10-3; 10-4; 10-5 моль/л.
Полученные стандартные растворы переносили в сухие химические стаканы на 50 мл №1, 2, 3, 4 и 5 соответственно, заполняя их на половину объема.
Подготовка водной вытяжки яблока
Для этого 20 г яблока измельчали на тёрке в ванночку. Взвешивали ванночку с яблоком с точностью ±0,01 г (ml). Шпателем переносили содержимое ванночки в центрифужную пробирку, доливали её дистиллированной водой приблизительно до ½ её вместимости, перемешивали стеклянной палочкой, палочку споласкивали водой. Взвешивали ванночку с остатками яблока (m2) и по разности между 1-м и 2-м взвешиванием вычислить массу взятого для анализа яблока m =m1-m2.
Содержимое пробирки центрифугировали сначала 5 мин. Жидкость из пробирки через воронку переносили в мерную колбу на 100 мл. К остатку в пробирке добавляли снова воды до ½ объёма и снова центрифугировали 2,5 мин. Жидкость опять сливали из пробирки в мерную колбу, доводили объём в ней до метки водой, перемешивали, переносили половину объема в сухой химический стакан № 5 на 50 мл и ионометрировали.
Ионометрическое определение содержания нитрат-ионов в яблоках
Для этого поочерёдно погружали подготовленные электроды гальванического элемента, составленного из индикаторного нитрат-селективного электрода и хлорсеребряного электрода сравнения, в каждый раствор в стаканах и измеряли ЭДС (Е), для каждого раствора стандартной серии и водной вытяжки. Измеренные величины Е для стандартной серии заносили в табл. 2.
Концентрация стандартного раствора | Е, В |
10-1 | 343,6 |
10-2 | 361,3 |
10-3 | 391,4 |
10-4 | 419,3 |
10-5 | 424,1 |
По данным табл. 1 строили градуировочный график зависимости E=f(pNO3), изображенный на рис. 1.
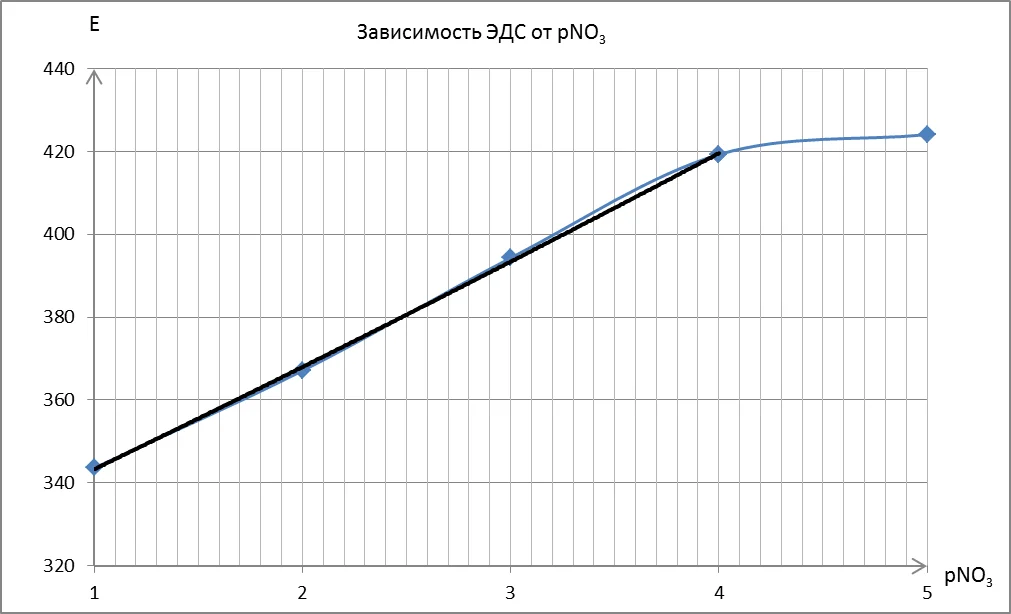
Затем с помощью графика определяли значение р(NO3) для каждой водной вытяжки и рассчитывали c(NO3), Т(NO3) и содержание нитрат-иона в мг/кг, используя массу яблока, взятую для анализа.
Параметры линейного уравнения регрессии: (с указанием доверительного интервала)
Коэффициент корреляции rxy = 0,9992.
Коэффициент детерминации R2 = 0,9984.
Остаточное стандартное отклонение sy=0,4443.
Стандартное отклонение методики sc=0,0174.
Средняя ошибка аппроксимации .
Результаты определения содержания нитрат-иона в яблоках представлены в табл. 3.
№ | Сорт яблок | Масса навески, г | Е, В | Содержание NO3-, мкг/кг |
1 | «Молдавия» | 21,290 | 412,1 | 22,60±0,34 |
2 | «Грени» | 20,263 | 426,0 | 5,44±0,09 |
3 | «Жигулевка» | 21,076 | 432,0 | 2,79±0,04 |
4 | «Александровка» | 21,226 | 433,0 | 2,54±0,05 |
5 | «Дочь папировки» | 20,889 | 442,0 | 1,00±0,02 |
6 | «Спартак» | 19,678 | 440,2 | 1,32±0,03 |
7 | «Гольден» | 19,854 | 437,1 | 1,74±0,04 |
8 | «Айдаред» | 20,341 | 441,3 | 1,12±0,02 |
9 | «Куйбышевское» | 20,450 | 407,5 | 39,96±0,44 |
10 | «Мантуан» | 20,868 | 423,2 | 7,27±0,12 |
Таким образом, содержание железа в исследованных сортах яблок соответствует норме, а содержание нитрат-ионов не превышает ПДК.